Análisis y síntesis elaborados por el staff médico de Circle Press

Secuestro mitocondrial: la evasión inmune antiviral
Sandra Milena Galvis, MD.
Médica cirujana, Universidad Industrial de Santander, Colombia.
La primera línea de defensa contra la infección viral está representada por el sistema inmune innato con el apoyo mitocondrial que, además, constituye la plataforma para la respuesta inmune adaptativa o adquirida. Ambas respuestas tienen como finalidad limitar la replicación viral y eliminar el agente infeccioso.
En mamíferos, la invasión microbiana no sólo desencadena la muerte celular programada de las células infectadas sino que también provoca una reacción inmune que está jerárquicamente organizada en una primera línea de respuesta provista por los efectores del sistema inmune innato (fagocitos infiltrantes y células natural killer) seguida por la activación de la inmunidad adaptativa mediada por los linfocitos T y B. El desequilibrio en la interacción entre el huésped y el agente patógeno viral es lo que conduce a la inmunopatogenia de las infecciones virales que puede derivar en enfermedad clínicamente aparente.
Las distintas estrategias por parte de los virus para la evasión inmunológica comprenden:
a) La interferencia con la presentación antigénica a través de moléculas HLA de clase I,
b) La disminución de la expresión de MHC (complejo mayor de histocompatibilidad) de clase II,
c) La disminución de la expresión de moléculas coestimuladoras,
d) La evasión de la respuesta de CTL (linfocitos T citotóxicos) mediante variación antigénica,
e) La evasión de la respuesta inmune a través de latencia viral y
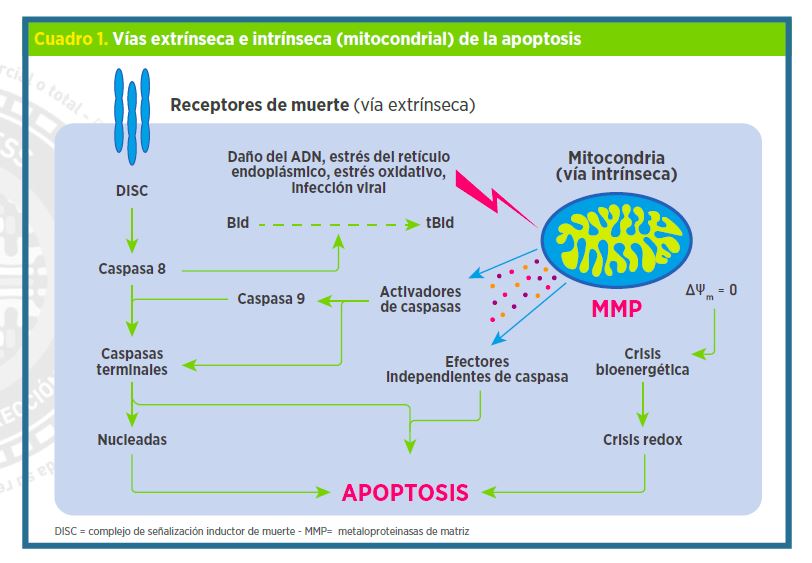
f) La interferencia con la apoptosis de las células infectadas (ver Cuadro 1).
La fusión y la fisión viral son procesos muy dinámicos. Los virus interfieren en estos procesos para distorsionar la dinámica mitocondrial con la finalidad de facilitar su proliferación. Por lo tanto, la interferencia en dichos procesos promueve alteraciones de las distintas vías de señalización celular1. En general, los virus ARN se identifican más con el proceso de generar apoptosis celular; en cambio, los virus ADN se identifican por generar procesos antiapoptóticos. Sin embargo, el virus de la hepatitis C es un virus ARN que genera un proceso antiapoptótico. Ahora bien, ¿cómo hace el virus para tomar el control de las células? Lo hace mediante el “secuestro mitocondrial”. El secuestro de la mitocondria interrumpe la función celular general y facilita que el virus controle la célula y pueda propagarse.
Varios estudios recientes han demostrado que las mitocondrias son los objetivos de las especies reactivas al oxígeno (ROS, por sus siglas en inglés) que se producen dentro de una célula durante las infecciones virales y que el ADN mitocondrial es un objetivo principal para estas ROS. Las especies reactivas al oxígeno interrumpen la producción oxidativa de ATP (adenosín trifosfato) que se requiere para la función celular normal porque el daño causado al ADN mitocondrial interrumpe, a su vez, la síntesis normal de proteínas necesarias para la función de las mitocondrias2.
Las numerosas funciones de las mitocondrias las hacen indispensables para la célula; entonces cuando un virus “secuestra” la función mitocondrial, esto le permite controlar toda la célula. Las mitocondrias desempeñan roles importantes en muchas vías de transducción de señales, en el proceso de envejecimiento, en la regulación de diferentes vías bioquímicas relacionadas con el metabolismo celular, en la patogénesis de numerosas enfermedades, en las respuestas inmunológicas y en el control del ciclo celular2.
El ADN mitocondrial es mucho más susceptible a la acción de las especies reactivas al oxígeno porque carece de histonas protectoras. Además, la mitocondria tiene enzimas de reparación del ADN con funciones más limitadas y está próxima a la cadena de transporte de electrones (ETC, por sus siglas en inglés) que representa el principal centro de producción de ATP y de ROS.
La medicina biorreguladora de sistemas puede aportar dos medicamentos importantes para mejorar el rendimiento de la mitocondria: Coenzyme Compositum™ y Ubichinon compositum™ (En Colombia, Heel 42 Solución Inyectable y Heel 177 Inyectable). El Coenzyme Compositum™ contiene todos los catalizadores del ciclo de los ácidos tricarboxílicos. El Ubichinon Compositum™ ayuda en la cadena respiratoria principalmente por su contenido de ubiquinona.
Además de las formas de administración ya conocidas para Coenzyme Compositum™ y Ubichinon Compositum™ en pacientes que refieren cansancio y agotamiento que les entorpecen el entrenamiento deportivo/ físico, estos medicamentos pueden administrarse por aspersión mucosa cada 15 minutos durante un período de 2 horas antes del entrenamiento físico.
En conclusión, los virus están preparados para quedarse en el organismo, pero este cuenta con herramientas para deshacerse de los virus, más aun si estas herramientas están respaldadas por fuentes exógenas.
Bibliografía:
1. Galluzzi L, Brenner C, Morselli E, Touat Z, Kroemer G. Viral control of mitochondrial apoptosis.
PLoS Pathog. 2008 May30;4(5):e1000018. doi:10.1371/journal.ppat.1000018.
2. Latif Reshi, Hao-Ven Wang, Jiann-Ruey Hong. Modulation of Mitochondria During Viral
Infections. Published: August 29th 2018 DOI: 10.5772/intechopen.73036.
Mitocondrias: los radares de la vigilancia inmune antiviral
Mónica Name Guerra, MD.
Medica cirujana, Universidad del Norte, Colombia.
La red mitocondrial representa la primera línea de defensa antiviral. Cuando una célula está expuesta a la invasión viral, hay ciertos sensores celulares que pueden detectar el material genético. Estos sensores son los receptores de reconocimiento de patrones (PRR, por sus siglas en inglés) asociados a patógenos (PAMP, por sus siglas en inglés), los cuales tienen un rol importante en el sistema inmune innato, a saber:
a) receptores toll (TLR, por sus siglas en inglés),
b) RIG-1, receptor citosólico inducible por ácido retinoico (RLR) y
c) receptores citosólicos del tipo de oligomerización de nucleótidos (NOD) (NLR).
Los receptores RIG-1 son los que están más estrechamente ligados a la activación de la función antiviral mitocondrial y detectan los virus ADN y ARN a nivel citoplasmático.
Durante la infección viral, los receptores de reconocimiento de patrones se ligan al ARN viral, permitiendo así su interacción con un adaptador polipeptídico mitocondrial (IPS-1 o MAVS) que es una proteína mitocondrial de señalización antiviral. La expresión de estas proteínas (MAVS/IPS-1) se ha detectado en la membrana externa de la mitocondria y promueve una cascada de factores de transcripción.
Estas proteínas activan factores de transcripción tales como:
a) el factor liberador de interferón 3 (IRF-3) y
b) el factor nuclear kappa beta (NF-kβ). Cuando estos factores de transcripción se activan, se produce una cascada de señales que conducen a la regulación positiva del interferón y de las citocinas proinflamatorias que, a su vez, induce el sistema inmune innato antiviral1.
Es decir que la proteína IPS-1/MAVS induce:
a) la transcripción nuclear para la producción de interferón tipo 1,
b) la expresión de receptores ligandos de linfocitos TCD8 citotóxicos y células natural killers, y
c) la apoptosis de células infectadas por el virus.
En resumen, los virus son los patógenos más abundantes sobre la Tierra y la sobrevida de muchos organismos dependerá de su habilidad para detectar y restringir la infección viral. La detección de los ácidos nucleicos es una manera fundamental de reconocimiento viral tanto en células eucariotas como en procariotas.
En los vertebrados, los receptores que censan ácidos nucleicos inducen la producción de interferón tipo 1 (IFN-1). Estas citocinas tienen varias funciones esenciales en la respuesta antiviral.
Los IFN-1 actúan tanto de una manera autocrina como paracrina, induciendo la expresión de cientos de genes que conjuntamente establecen un “estado antiviral” que restringe la diseminación del virus hacia células vecinas.
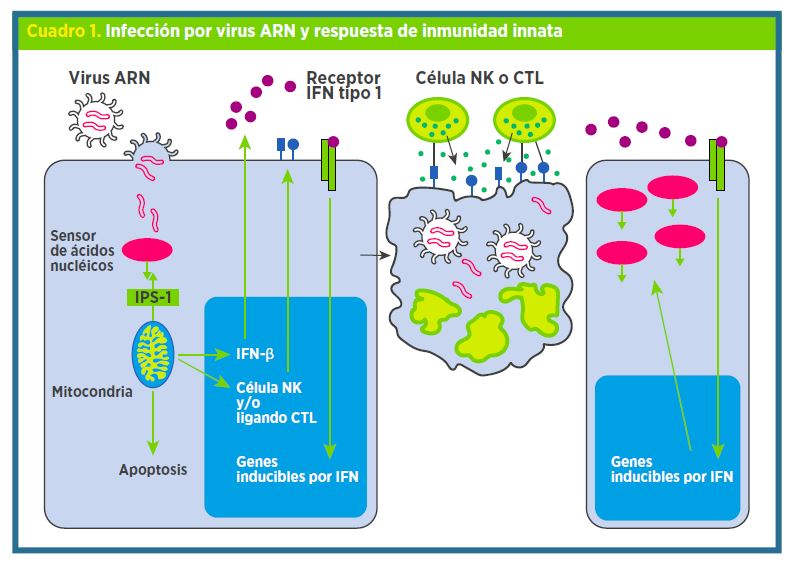
Además, el IFN-1 estimula la función de las células natural killers (NK) y la diferenciación de los linfocitos T citotóxicos específicos del virus (CTL), que son los que reconocen y eliminan las células infectadas por el virus (ver Cuadro 1)1.
En las mitocondrias que presentan alteraciones, esta línea de defensa antiviral a través de la producción de IFN-1 se pierde. Si se aporta interferón en forma exógena, sólo se reinstaura la respuesta celular independiente del mecanismo de IPS-1, es decir, se reinstaura una respuesta mediada por los genes inducibles de IFN. Vale decir que desde el punto de vista clínico, es más útil tratar de restaurar las funciones mitocondriales que suministrar un aporte exógeno de IFN.
Hay otras 2 proteínas asociadas a las funciones antivirales de las mitocondrias (STING y MFN2) que se encuentran localizadas en el retículo endoplásmico y conducen a la producción de IFN-β. Estas proteínas funcionan como adaptadores moleculares para mediar la señalización en los sitios de contacto entre las mitocondrias y el retículo endoplásmico, lo cual sugiere que estos sitios de contacto entre mitocondrias y retículo endoplásmico desempeñan un papel crítico como mediadores de señales durante las respuestas antivirales llevadas a cabo por la célula huésped2.
El virus de la hepatitis C, por ejemplo, produce la escisión de MAVS con la finalidad de evitar una respuesta viral potente y así poder evadirla. La desregulación de la inmunidad antiviral también ha sido sugerida por el hallazgo de anticuerpos dirigidos a los componentes mitocondriales.
En síntesis, es posible afirmar que la desregulación mitocondrial altera la respuesta inmune antiviral. Por lo tanto, ante una infección viral, pueden administrarse medicamentos que hacen blanco en las redes biológicas para reforzar la capacidad autorreguladora del organismo. La medicina reguladora de sistemas ofrece 2 de estos medicamentos: a) Coenzyme Compositum™ y b) Ubichinon Compositum™.
El Coenzyme Compositum™ estimula por medio de catalizadores el ciclo de los ácidos tricarboxílicos de Krebs mientras que el Ubichinon Compositum contiene todas las citocromo-oxidasas que activan la cadena respiratoria mitocondrial.
El Coenzyme Compositum™ contiene beta vulgaris conditiva B4 que en algunos trabajos de investigación ha demostrado tener capacidad antioxidante, antiviral y antibacteriana proveniente de las betalaínas (betacianinas y betaxantinas). El Ubichinon Compositum™, el cual mejora toda la cadena respiratoria, está compuesto por cofactores intermediarios tipo quinonas que aumentan la transferencia de electrones. Además, contiene Podophyllum peltatum que posee ligandos y glucósidos con capacidad de inhibir el ensamblaje de los microtúbulos durante la mitosis y la síntesis de ADN mediante la inhibición de las topoisomerasas I y II. Presenta actividad antiviral contra el sarampión, el herpes simple tipo 1 y el virus del papiloma humano.
Asimismo, el Ubichinon Compositum™ contiene antraquinona que es un pigmento fenólico proveniente de plantas, se encuentra en diferentes hierbas y vegetales y tiene actividad antiviral por su efecto viricida.
La hipericina presenta actividad contra el virus del herpes simple 1 y 2, los virus de la parainfluenza y el virus de la estomatitis vesicular. El ácido crisofánico presente en la antraquinona inhibe la replicación de los polivirus tipo 2 y 3 mientras que la emodina ha sido eficaz contra los virus con envoltura como el virus de la varicela-zóster, el virus de la gripe, los virus del herpes simple 1 y 2 y el virus de la hepatitis B.
En conclusión:
• Las mitocondrias son orgánulos claves para la inmunidad innata que activan la producción de los interferones tipo 1 (IFN-α e IFN-β).
• Los medicamentos biorreguladores mitocondriales como el Coenzyme Compositum™ y el Ubichinon Compositum™, a través de la optimización de las funciones metabólicas y energéticas de las mitocondrias, podrían ayudar a reforzar la respuesta inmune antiviral.
• La administración de estos medicamentos permitiría: a) acortar la duración de los síntomas y b) evitar que los virus evadan la respuesta inmunológica y, por ende, evitar la cronicidad, la recurrencia y la progresión de los procesos virales.
• Estos medicamentos pueden administrarse por vía parenteral o por vía oral. En niños, pueden administrarse mediante nebulizaciones.
Bibliografía:
1. Stetson DB, Medzhitov R. Antiviral defense: interferons and beyond [published correction appears in J Exp Med. 2006 Sep 4;203(9):2215]. J Exp Med. 2006;203(8):1837-1841. doi:10.1084/jem.20061377.
2. Ohta A, Nishiyama Y. Mitochondria and viruses. Mitochondrion. 2011;11(1):1-12. doi:10.1016/j. mito.2010.08.006.
3. Saitoh, T., Akira, S. Regulation of innate immune responses by autophagy-related proteins. J. Cell Biol. 2010;189:925–935.
4. van Vliet AR, et al. New functions of mitochondria associated membranes in cellular signaling. Biochimica et Biophysica Acta 1843 (2014)2253–2262.
5. Bansal AS, et al. Chronic fatigue syndrome, the immune system and viral infection. Brain Behav Immun. 2012;26:24–31.
6. Bedows E, Hatfield GM. An Investigation of the Antiviral Activity of Podophyllum peltatum. J Nat Prod. 1982;45(6):725-729.
7. Andersen DO, Weber ND, Wood SG, Hughes BG, Murray BK, North JA. In vitro virucidal activity of selected anthraquinones and anthraquinone derivatives. Antiviral Res. 1991;16(2):185-196.
8. Semple SJ, Pyke SM, Reynolds GD, Flower RL. In vitro antiviral activity of the anthraquinone chrysophanic acid against poliovirus. Antiviral Res. 2001;49(3):169-178.
9. Ravichandran K, et al. Impact of processing of red beet on betalain content and antioxidant activity. Food Research International 2013;50:670–675.
Disfunción mitocondrial, estrés oxidativo: su papel en la tormenta de citoquinas
Enrique Terán, MD.
Colegio de Ciencias de la Salud, Universidad San Francisco de Quito, Ecuador.
La mitocondria es una organela que ocupa una porción sustancial del volumen citoplasmático en las células eucariotas y ha sido esencial para la evolución de los animales complejos. La función principal de la mitocondria (aunque no es la única función) es la síntesis de ATP (adenosín trifosfato) a partir del ADP (adenosín difosfato) y del fósforo inorgánico por el proceso de fosforilación oxidativa. Sin mitocondrias, las células animales serían actualmente dependientes de la glucólisis anaerobia para toda su síntesis de ATP. Sin embargo, cuando la glucosa se convierte en piruvato por medio de la glucólisis, sólo se libera una pequeña fracción de la energía total, potencialmente disponible1.
Existen 4 procesos claves interrelacionados. El primero de ellos es la glucólisis que lleva la glucosa a piruvato. El segundo es la oxidación del piruvato que da lugar a la formación de acetil-CoA, el cual es el sustrato fundamental para el ciclo de los ácidos tricarboxílicos (tercer proceso) para finalmente llegar a la fosforilación oxidativa, es decir, a la cadena respiratoria mitocondrial (cuarto proceso)1.
En la mitocondria, el metabolismo del azúcar es complejo. El piruvato es importado a la mitocondria y oxidado por el oxígeno molecular, dando como resultado CO2 y H2O. La energía liberada se aprovecha en forma eficiente con 36 moléculas de ATP generadas por cada molécula de glucosa oxidada.
Por el contrario, solo 2 moléculas de ATP se producen por la glucólisis sola. Es decir que la glucólisis tiene baja capacidad energética mientras que la fosforilación oxidativa tiene como resultado una producción masiva de energía a partir del mismo sustrato.
Para la síntesis de ATP, los electrones son transportados organizadamente a partir de 2 precursores comunes que son el NADH (nicotinamida-adenina-dinucleótido reducida) y el FADH2 (flavin-adenina-dinucleótido reducida) que provienen del ciclo de los ácidos tricarboxílicos o ciclo de Krebs (localizado en la matriz mitocondrial), de la glucólisis (localizada en el citoplasma) y la oxidación de los ácidos grasos por O2.
Vale decir que la glucólisis puede aportar NADH al igual que la oxidación del piruvato mientras que el ciclo de Krebs aporta una masiva cantidad de NADH y una pequeña cantidad única de FADH2.
Dado que los electrones no se crean o destruyen en las reacciones químicas, si una molécula se oxida, otra deberá reducirse (reacción redox). En consecuencia, por definición las reacciones de óxido-reducción son transferencias de electrones. En una reacción redox1: NADH + H+ + (1/2) O2 ↔↔ NAD+ + H2O. Es decir que cuando el NADH se oxida a NAD+ (pierde electrones), el oxígeno molecular se reduce a agua (gana electrones). Sin embargo, los electrones no son transferidos desde el NADH al oxígeno en forma directa, sino que lo hacen mediante una cadena de portadores de electrones conocida como “cadena transportadora de electrones” y también denominada cadena respiratoria.
Es importante mencionar que el complejo I y el complejo II son independientes y, por lo tanto, los electrones “saltan” del complejo I al complejo III (y también del complejo II al complejo III). Es por eso que el NADH actúa sobre el complejo I mientras que el FADH2 actúa sobre el complejo II.
También es importante destacar que, para que el electrón pueda ser transferido de un complejo a otro, necesita un intermediario que en el caso de los complejos I y II es la ubiquinona o la coenzima Q (que en células de mamíferos es la coenzima Q10 por la extensión de carbonos que posee). Esta coenzima Q tiene un estado oxidado y otro reducido, y estos 2 estados dependerán del número de electrones que vayan a ser aportados.
Del complejo III al complejo IV, el transporte de electrones se lleva a cabo por el citocromo C y es cuando se alcanza el último estadio con generación de energía (y producción de agua). Entonces, la fosforilación oxidativa tiene lugar a partir de complejos de proteínas que están localizados en la membrana mitocondrial interna, los cuales incluyen los complejos I-IV de la cadena respiratoria de transporte de electrones, la ATP sintasa (complejo V) y la translocasa de los nucleótidos de adenina (ANT).
Existe una relación entre las mitocondrias y la respuesta inmune innata. Múltiples estudios han establecido una relación entre las vías de señalización de los receptores de la inmunidad innata (receptores para reconocimiento de patógenos) y la mitocondria.
Algunos patógenos han desarrollado estrategias para modificar la dinámica mitocondrial que los beneficie porque la mitocondria puede llegar a producir especies reactivas al oxígeno (ROS, por sus siglas en inglés) que son dañinas para la sobrevida y/o proliferación de patógenos intracelulares2.
Algunos agentes patógenos como el Helicobacter pylori, la Shigella, la Chlamydia, algunos virus como el de la influenza, el dengue, el HIV y los virus respiratorios como el SARS ingresan a la célula.
El Helicobacter, cuando infecta la célula, produce una citotoxina vacuolizante (vacA) que genera fragmentación mitocondrial que produce la liberación del citocromo C hacia el citosol que, al ser tóxico, conduce a la muerte celular.
La Listeria, en cambio, secreta una toxina denominada listeriolisina O, la cual hace que se formen poros que conducen también a la fragmentación de la mitocondria que es independiente de la proteína DRP-1* pero produce la misma consecuencia que es la muerte celular. La Shigella y la Legionella producen fragmentación mitocondrial dependiente de DRP-1* llevando a la muerte celular. Es decir que estas 4 bacterias terminan de una forma común que es la muerte celular para evitar que la producción de radicales libres las dañe.
En cambio, la Chlamydia lleva a la fusión mitocondrial que va a depender de la energía que se puede producir a nivel intracelular y que es necesaria para su proliferación intracelular.
El virus del dengue inhibe la proteína DRP-1*, evitando así la fragmentación mitocondrial que necesita para su replicación, también para la respuesta inmune y posterior evasión inmunitaria por parte del virus.
El virus del síndrome respiratorio severo agudo (SARS, por sus siglas en inglés) y el virus del HIV causan degradación de DRP-1* y evitan la fragmentación mitocondrial. Vale decir que los 3 virus descriptos no causan muerte celular y además, estimulan la proliferación de mitocondrias (y, por ende, de radicales libres).
El Mycobacterium tuberculosis aumenta la glucólisis aeróbica principalmente en las células epiteliales y en las células inmunológicas que presentan una disminución del ciclo de Krebs con el consiguiente aumento del flujo glucolítico. Vale decir que el M. tuberculosis aumenta la glucólisis intracelular al mismo tiempo que bloquea el ciclo de los ácidos tricarboxílicos, por lo cual la mayor cantidad de piruvato producida va a generar lactato.
La brucelosis promueve la producción de lactato a través de la glucólisis aeróbica mientras que a la vez suprime el ciclo de Krebs, lo cual finalmente conduce a la acidosis láctica.
La Chlamydia aumenta los niveles del transportador de glucosa GLUT-1, favoreciendo una mayor captación de glucosa con incremento del flujo glucolítico que es necesario para su crecimiento intracelular.
El Herpesvirus induce el ciclo de los ácidos tricarboxílicos promoviendo una mayor respiración celular.
El virus de la hepatitis C altera la oxidación mitocondrial de los ácidos grasos, estimulando una mayor producción de energía a partir de una fuente alternativa como son los ácidos grasos.
Una vez que la célula se encuentra infectada (por Helicobacter, Shigella, Mycobacterium, etcétera), se produce daño mitocondrial que, a su vez, conduce a la degradación mitocondrial que finalmente deriva en la apoptosis celular. Mientras que, por ejemplo, Chlamydia y Legionella bloquean la vía de la muerte celular mitocondrial para promover su proliferación intracelular.
El virus de la influenza A, en cambio, aumenta la muerte celular porque este hecho lo ayuda a diseminarse. El virus del Zika bloquea la muerte celular, creando reservorios intracelulares que permiten a los viriones salir a infectar otras células.
En resumen, el proceso de infección celular crea un daño ultraestructural que lleva a la disfunción mitocondrial con una disminución del potencial de membrana mitocondrial, lo cual, a su vez, tiene un doble impacto:
a) disminuye la producción de energía, es decir, disminuye la síntesis de ATP y
b) aumenta la generación de especies reactivas al oxígeno (ROS) y radicales libres.
Las ROS son especies químicas intracelulares reactivas a los lípidos, las proteínas y los ácidos nucleicos. Estas ROS incluyen:
a) el anión superóxido (O2 -),
b) el peróxido de hidrogeno (H2O2) y
c) los radicales hidroxilo (OH-).
La superóxido dismutasa convierte rápidamente el O2 – en H2O2 porque el O2 – puede dañar las proteínas que contienen puentes de hierro-sulfuro (por ejemplo, el glutatión). El H2O2 puede modular señales para oxidar los tioles dentro de las proteínas.
Cuando la actividad mitocondrial se encuentra afectada y no hay un proceso adecuado de transporte de electrones debido a un aprovisionamiento incompleto o a un reciclaje no adecuado de los transportadores, se generan especies reactivas al oxígeno (ROS) que tendrán 3 acciones fundamentales:
a) generar una adaptación metabólica,
b) producir diferenciación celular y
c) afectar la proliferación celular.
Una especie reactiva al oxígeno que ha surgido recientemente es el óxido nítrico que, si bien desempeña un papel fisiológico en la vasodilatación vascular y la agregación plaquetaria, también cumple un rol importante en la respuesta inmunológica con la citotoxicidad inducida por óxido nítrico.
El exceso de radicales libres junto con el exceso de óxido nítrico puede ser problemático porque cuando hay formación de radical superóxido, el óxido nítrico reacciona con este radical, generando peroxinitrito que es un ROS más dañino que el anión superóxido.
El peroxinitrito no sólo daña la célula, sino que también produce daño a nivel mitocondrial, afectando la función de los complejos I y II y también la función de la ATP-sintasa.
En consecuencia, cuando se afecta la función mitocondrial, hay un estímulo para la formación de mediadores inflamatorios. En caso de infecciones virales respiratorias, la activación de mediadores inflamatorios conduce a la formación de citoquinas, es decir que existe una correlación directa entre el mal funcionamiento mitocondrial y el estímulo a la producción de citoquinas.
La tormenta de citoquinas es un proceso que tiene como base una alteración génica que lleva a una sobreproducción de estos mediadores de inflamación que aumentan en forma desmedida.
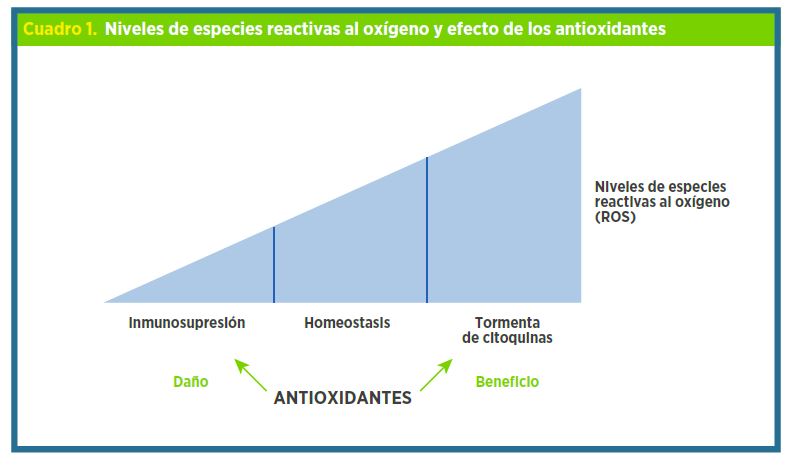
El concepto fundamental es que, cuando hay un estado de homeostasis, los antioxidantes controlan los radicales libres, pero cuando los niveles de radicales libres aumentan desmesuradamente, se produce la tormenta de citoquinas y es en este momento donde el aprovisionamiento de antioxidantes tendrá un papel beneficioso para tratar de controlar el proceso (ver Cuadro 1). Por el contrario, en estados de inmunosupresión, la provisión de antioxidantes puede desempeñar un papel discutido porque pueden afectar la limitada capacidad de defensa que posee el organismo.
En conclusión:
• La actividad mitocondrial es fundamental para la homeostasis celular.
• La presencia de patógenos en el organismo produce cambios en la actividad mitocondrial.
• En muchos casos, la mitocondria produce mayor cantidad de radicales libres (ROS).
• Los ROS, a su vez, están vinculados con un aumento en la generación de citoquinas
proinflamatorias.
• La tormenta de citoquinas puede ser la vía final de toda esta cadena de procesos.
Bibliografía:
1. Molecular Biology of the Cell, 4th edition. Bruce Alberts, Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, and Peter Walter. New York: Garland Science; 2002.
2. West AP, Shadel GS, Ghosh S. Mitochondria in innate immune responses. Nat Rev Immunol. 2011;11(6):389-402. doi:10.1038/nri2975.

Material exclusivo para el profesional de la salud. © 2020 Circlepress. All rights reserved.