
Actualmente, es evidente la presencia de enfermedades alérgicas e infecciones respiratorias en todas las comunidades a nivel mundial, y se ha convertido en uno de los principales motivos de consulta tanto ambulatoria como hospitalaria. Las poblaciones en riesgo, como ancianos, menores de edad y mujeres embarazadas son las que tienen mayor vulnerabilidad y riesgo de complicación cuando padecen alguna de estas afecciones. 1 Este tipo de enfermedades, cuya prevalencia va en aumento e impacta en la salud pública, asociado directamente a factores de riesgo medioambientales, constitucionales y epigenéticos, hace que exista una necesidad permanente de implementar estrategias terapéuticas que van de lo preventivo a lo curativo, en la mayoría de los casos con tratamientos concertados en diferentes guías o protocolos de manejo a nivel mundial. Asimismo, se permite la oferta de múltiples medicamentos orales, tópicos, inyectables e inhaladores, agrupados de manera general en antihistamínicos, antibióticos, antiinflamatorios, antivirales, hidratantes, corticoesteroides y biológicos.
Sin embargo, estas enfermedades alérgicas y respiratorias se convierten cada día en un gran reto terapéutico para el gremio médico, sobre todo, si se tiene en cuenta factores claves, como una mayor exposición a alérgenos, agentes xenobióticos, patrones moleculares asociados al daño (Danger associated mollecular patterns, DAMPS) o agentes patógenos exógenos (Exogenous microbe associated mollecular patterns, MAMPS)2; presencia de niveles elevados de cortisol asociados al estrés; dietas poco saludables con alto consumo de azúcar y grasas; uso o abuso de antibióticos. Todos estos factores están relacionados directamente con perturbaciones de la respuesta inmunológica, en especial, con respuesta innata, inmunosenescencia y estados de inflamación crónica de bajo grado2,3, que hacen que el manejo de este tipo de enfermedades alérgicas y respiratorias no sea fácil, y que presente muchas veces un alto índice de fracaso terapéutico y la aparición de brechas terapéuticas. Estas brechas pueden ser, por nombrar algunas, falta de medicamentos que disminuyan una carga viral cuando la infección es por virus, no contar con medicamentos que biorregulen la respuesta del sistema inmunológico hacia la protección antiviral o en la modulación de la respuesta alérgica, no tener medicamentos que busquen una respuesta fisiológica (autorregulación) más que farmacológica, para que los beneficios superen los riesgos (efectos secundarios), y no contar con medicamentos que abarquen diferentes dianas terapéuticas, caracterizados por su efecto sinérgico.
Esta condición ha permitido que se abra la oportunidad de un manejo integral para este tipo de patologías a través del uso de medicamentos biorreguladores, multiobjetivo y multicomponente, en dosis bajas, que van más allá del manejo de los síntomas comunes (como fiebre, dolor, inflamación, exudación, edema y picazón) y buscan respuestas para la autorregulación de redes biológicas afectadas en estas condiciones de enfermedad, como lo es la respuesta inflamatoria a través de la modulación en la producción de citoquinas proinflamatorias necesaria en el control de procesos alérgicos inflamatorios de la piel o de las vías respiratorias, o la acción inmunomoduladora y protectora de la mucosa necesaria en el manejo de afecciones como la rinosinusitis, e incluso, la acción inmunoestimulante de origen natural en el manejo de la infección respiratoria aguda, principalmente de etiología viral.
Dr. Baltazar Guerrero Quesada
Médico Cirujano General, Escuela de Medicina Juan N. Corpas. Especialista en Administración, Universidad Santo Tomás. Especialista en Calidad en Salud, Universidad El Bosque. Médico Epidemiólogo, Universidad del Rosario. Especialista en Terapias Alternativas y Farmacología Vegetal, Universidad Juan N. Corpas, Miembro activo de la Sociedad Colombiana de Medicina China y Acupuntura. Magister en Fitoterapia Clínica, Universidad de Barcelona, España.
Bibliografía
1. Simon F. Thomsen. Epidemiology and natural history of atopic diseases.
European Clinical Respiratory Journal. 2015.2:24642.
2. Ronan kapetanovic. Innate immune perturbations, accumulating DAMPs
and inflammasome dysregulation: a ticking time bomb in ageing. Ageing
Research Reviews. 2015; 24:40-53.
3. Matthew C. Morris, Elizabeth A. Gilliam2 and Liwu Li Innate immune
programing by endotoxin and its pathological consequences. January 2015,
Volume 5, Article 680.
Euphorbium compositum®
Controle eficazmente la obstrucción nasal de forma natural1
Las vías aéreas superiores se ven afectadas con frecuencia por diferentes eventos inflamatorios, como rinitis (inflamación de la mucosa nasal), sinusitis (inflamación de senos paranasales) y rinosinusitis (inflamación de nariz y senos paranasales simultáneamente).
La sinusitis coexiste, por lo general, con la rinitis y es lo que, comúnmente, se conoce como rinosinusitis; sin embargo, la sinusitis puede presentarse como una patología única. Ambas provocan síntomas físicos considerables que afectan de manera importante la calidad de vida.
La rinosinusitis (RS) se caracteriza por la presencia de 2 o más síntomas, como bloqueo/obstrucción nasal, rinorrea, picazón, dolor facial, sensación de presión nasal, reducción de olfato y tos en niños. Se puede asociar a pólipos nasales y/o secreción mucopurulenta, así como alteraciones del complejo osteomeatal de los senos. La RS puede ser aguda (menor a 12 semanas) o crónica (mayor a 12 semanas). Las causas pueden ser alérgicas y no alérgicas. Entre las primeras, encontramos alérgenos, como polen, ácaros del polvo doméstico, mohos, mascotas. Entre las causas de las no alérgicas, infecciones virales, irritantes (lejía, aire frío, ejercicio), hormonas (embarazo, hipotiroidismo), comidas especiadas, fármacos (anticonceptivos orales, antihipertensivos, psicotrópicos, AINES), uso indebido de descongestivos nasales, trastornos inflamatorios- inmunológicos (desencadenantes indeterminados o mal definidos).2,3,4,5
La inflamación alérgica y las infecciones del tracto respiratorio superior son afecciones que parecen fomentarse y reforzarse mutuamente. Un pequeño porcentaje de pacientes con rinosinusitis posviral aguda tendrá rinosinusitis bacteriana aguda (ver Cuadro 1).6
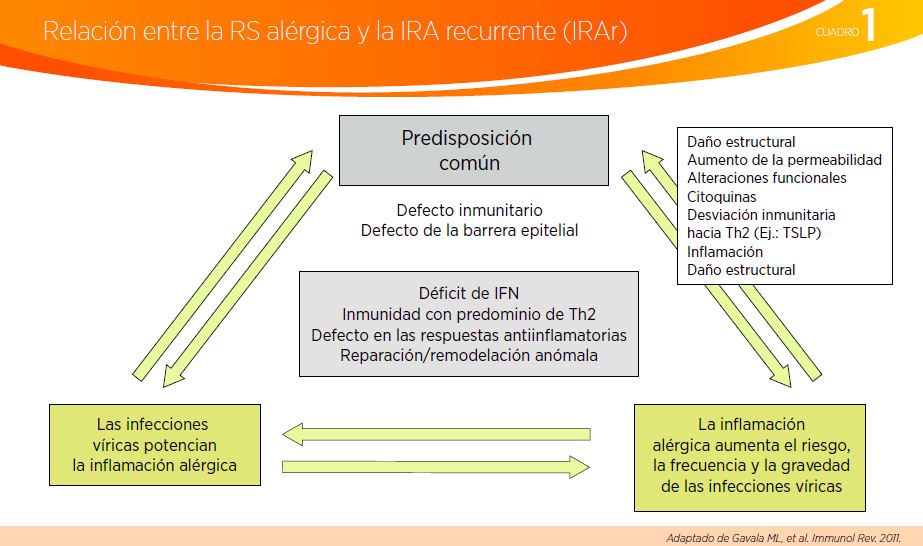
El tratamiento habitual de la RS alérgica consiste en terapias tópicas, como corticoides intranasales, antihistamínicos, cromoglicato de sodio y bromuro de ipratropio. La terapia sistémica incluye antihistamínicos, antagonistas de leucotrienos y corticoides orales. Otra opción es la inmunoterapia de desensibilización (3-5 años) o descongestivos sistémicos (ver Cuadro 2).2

Estas terapias farmacológicas tienen diferentes efectos adversos de acuerdo con el medicamento y el tiempo de uso: somnolencia, hemorragia nasal, perforación del tabique, hipertensión, palpitaciones, insomnio, sequedad nasal, cefalea y síntomas gastrointestinales. 7
Ante las limitaciones del uso de medicamentos convencionales por el efecto rebote, la imposibilidad de uso a largo plazo, los efectos adversos y las contraindicaciones en niños, existe la posibilidad de mejorar el tratamiento de la rinitis, sinusitis y rinosinusitis con Euphorbium compositum®.
Euphorbium compositum® es un inmunomodulador antiviral que favorece la función de la mucosa gracias a sus efectos antivirales y antiinflamatorios6,7. Las presentaciones de Euphorbium compositum® son spray nasal, gotas orales y ampollas.
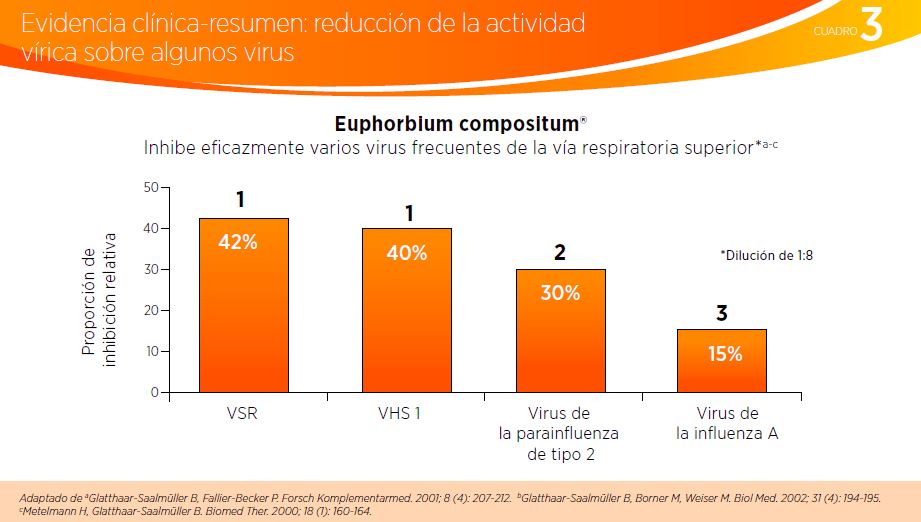
La actividad antivírica de Euphorbium compositum® frente a los patógenos normalmente responsables de las infecciones de la vía respiratoria superior se ha investigado en tres estudios de reducción de placas de virus in vitro8,9,10. Las propiedades antivirales se deben a un mecanismo antigénico inespecífico, y se cree que esta acción amplifica el sistema de defensa natural del cuerpo, basado en el interferón (IFN).10
La evidencia clínica mostró que el Euphorbium compositum® redujo la actividad viral del VSR (virus sincitial respiratorio), del VHS1 (virus herpes simplex 1), virus parainfluenza tipo 2 y virus de la influenza A (ver Cuadro 3).
También, se valoraron los efectos inmuno-farmacológicos del Euphorbium compositum® en una aproximación de las condiciones in vivo. Varios de sus componentes son farmacológicamente potentes sobre determinados mediadores citocínicos: interferon-gamma (INFγ), TNF-α IL-10. Los datos indican que se alcanza un efecto del ≥20% (efecto a nivel farmacológico) sobre estos mediadores con estos componentes.11
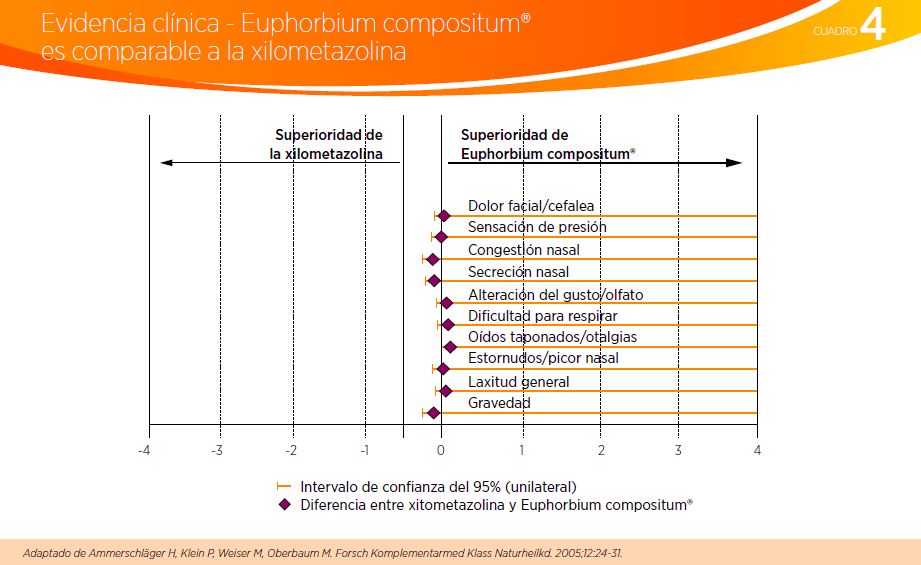
Además, se observó una eficacia comparable en cuanto a la reducción de síntomas con Euphorbium compositum® en spray nasal comparado con otras alternativas terapéuticas, como la xilometazolina. Después de crear niveles de propensión, se advirtió la no inferioridad en todas las variables; en ningún caso, cruzó el límite del intervalo de confianza del 95%, además no se observó el efecto de rebote dado por la suspensión de la xilometazolina. (ver Cuadro 4).
En la sinusitis crónica, el Euphorbium compositum® mejoró significativamente los síntomas en 4 semanas frente al placebo (mediana de 21.1% vs. 14.3%, p=0.015). La evaluación realizada por los pacientes sobre el uso de Euphorbium compositum® en spray nasal reveló una satisfacción muy buena en el 80.8% (las opciones fueron muy bueno, satisfactorio, sin mejora o empeoramiento sintomático).12 En niños de 2-6 años de edad, el 97% de los médicos y el 96% de los padres comunicaron tolerabilidad muy buena o buena con Euphorbium compositum® en nebulizador nasal (ver Cuadro 5).

Euphorbium compositum® ha sido investigado durante más de 20 años y tiene un amplio uso en pacientes de más de 30 países. Ejerce acción múltiple sobre los virus comunes de las vías respiratorias superiores y sobre los mediadores antiinflamatorios, además de apoyar la función de la mucosa. La seguridad y eficacia científica fueron clínicamente demostradas, con una buena base de estudios y publicaciones en pacientes de todas las edades con rinitis/sinusitis/rinosinusitis de diversa etiología.
Demostró la misma eficacia que la xilometazolina en sinusitis y rinitis, pero con mejor tolerancia. Es seguro para usar en toda la familia, adultos y niños con dichas afecciones, sin efecto de rebote ni taquifilaxia ni efectos secundarios raros. Tampoco se observaron contraindicaciones importantes ni interacciones farmacológicas conocidas. Euphorbium compositum® ofrece la mejor alternativa natural ante los tratamientos médicos convencionales (ver Cuadro 6).

Bibliografía:
1. Gottwald R, Weiser M. Antihomotoxic treatment at Chronic sinusitis.
Medicina Biológica. Vol 14 N° 1, 2001, PP. 4-7.
2. Fokkens WJ, et. al. Rhinol Suppl 2012(23):1-298.
3. Dykewicz MS, et al. Allergy Clin Immunol 2010;125(2 Sppl 2):S103-115.
4. Jovancevic L, et. al. Rhinology 2010;48(1):7-10.
5. Ramey JT, et.al. J Investig Allergol Clin Immunol 2006;16(3):148-155.
6. Gavala ML, et. al. Immunol Rev 2011.
7. Hermann Ammerschläger, et. al. Forsch Komplementarmed Klass
Naturheilkd. 2005 Feb;12(1):24-31.
8. Glatthaar-Saalmuller B, et. al. Biol med 2002;31(4):194-195.
9. Metelmann H, et. al. Biomed Ther 2000;18(1):160-164.
10. Glatthaar-Saalmuller B, et. al. Forsch Komplement 2001;8(4):207-212.
11. Schmolz M, et. al. Biol Ther 1999;17(2):61-63.
12. Zenner S, et. al. Hufeland J 1992;7(3):67-74.
Engystol®
Eficaz para la prevención y tratamiento de infecciones virales1,2
La infección respiratoria aguda (IRA) es toda patología que se presenta con menos de 15 días de evolución, y que tiene origen infeccioso. Dentro de los síntomas más frecuentes se encuentran tos, disnea, rinorrea, obstrucción nasal, coriza, fiebre, odinofagia, otalgia, signos y síntomas tanto locales como generalizados cuya intensidad está asociada con la severidad del cuadro. Las personas, a lo largo de la vida, son susceptibles de sufrir IRA. Su transmisión es frecuente de persona a persona a través de la inhalación de aerosoles, gotas con gérmenes provenientes de personas infectadas o de fómites. Diversas entidades clínicas están incluidas en el grupo de la IRA: rinofaringitis, faringoamigdalitis, bronquiolitis, neumonía, crup, entre otras (ver Cuadro 1).3

La etiología de la IRA comprende diversos agentes, como virus, bacterias, hongos y hasta parásitos; los dos primeros son los más frecuentes y en la población pediátrica, la causa viral es la predominante.3 Los virus implicados son virus sincitial respiratorio (VSR), influenza, parainfluenza, rinovirus, adenovirus, enterovirus, coronavirus, y los más recientemente identificados: el bocavirus y metapneumovirus.3 Estos pueden estar solos, asociados o en combinación con agentes bacterianos. La infección respiratoria aguda es una de las primeras causas de atención médica en todo el mundo, tanto en la consulta ambulatoria como en la hospitalización, y se encuentra entre las primeras causas de mortalidad en niños menores de 5 años y en adultos mayores de 65 años. En Colombia, es uno de los eventos vigilados a través del Sistema Nacional de Vigilancia en Salud Pública (SIVIGILA), lo que permite la identificación oportuna de cambios en la endemicidad para orientar las intervenciones de promoción, prevención y atención en los servicios de salud.4
En el boletín epidemiológico del Instituto Nacional de Salud (BES), en la semana epidemiológica 12 de 2018, fueron notificados en el sistema de vigilancia un total de 1.420.961 consultas externas y urgencias por IRA y 52.755 hospitalizaciones por IRAG, con una disminución del 11.8% en las consultas externas y urgencias por IRA y del 9.0% en las hospitalizaciones por IRAG notificadas el año anterior. Desde la semana epidemiológica 7, las consultas externas y las urgencias por IRA superan el umbral estacional y se encuentran por debajo del límite superior histórico.
Actualmente, la morbilidad por IRA ha superado el promedio histórico de la morbilidad de 2013 a 2017. Las precipitaciones acordes con las predicciones climáticas son uno de los factores que favorece este aumento en la mayor parte del territorio nacional.
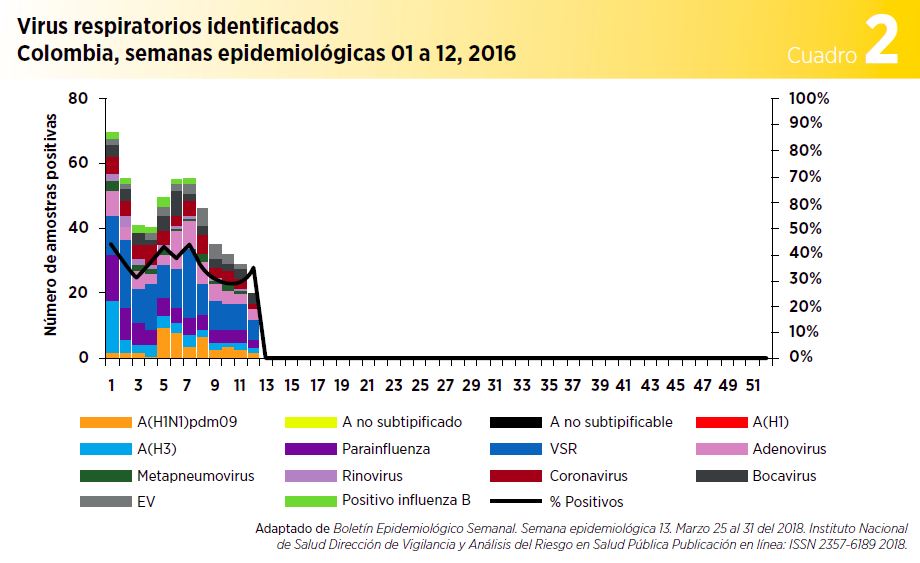
Según la información consolidada de los resultados de inmunofluorescencia y RTPCR de las muestras procesadas por los Laboratorios de Salud Pública Departamentales y el Laboratorio de Virología del INS, la semana epidemiológica 12 de 2018, el virus sincitial respiratorio corresponde al 26.8% del total de muestras positivas, seguido por parainfluenza con el 13.9%, adenovirus con el 12.0%, subtipo de influenza A/H3 con el 8.0%, influenza A(H1N1)pdm09 con el 9.1%, coronavirus con el 9.3%, virus bocavirus con el 8.4%, enterovirus con el 4.8%, metapneumovirus con el 3.4%, rinovirus con el 2.7% e influenza B con el 1.7% (ver Cuadro 2).5
Debido a la fácil trasmisión, la alta morbimortalidad, así como la carga que representa para el sistema de salud, es muy importante promover acciones básicas encaminadas a la prevención de esta patología. Las medidas más recomendadas son la lactancia materna, el lavado de manos, el uso de alcohol glicerinado, la vacunación y la educación a la población respecto a la prevención y a los signos de alarma para la consulta temprana.
Como la principal causa de esta patología es de origen viral y su cuadro clínico es tan incapacitante, el manejo farmacológico es en su mayoría solo sintomático e incluye antipiréticos, analgésicos, antitusivos, mucolíticos, expectorantes, corticoides, broncodilatadores y antihistamínicos, frecuentemente automedicados y acompañados con el uso indiscriminado de antibióticos, que pueden aumentar los riesgos de efectos adversos a los medicamentos y el incremento de la resistencia bacteriana, y genera así un nuevo problema de salud pública. Por otra parte, existen varias sustancias disponibles para el tratamiento efectivo de infecciones virales, como la amantadina, inhibidores de la neuraminidasa y análogos de nucleósidos. Sin embargo, muchas sustancias antivirales están asociadas con efectos secundarios, por eso, se necesitan sustancias antivirales que tengan buena eficacia y tolerabilidad y baja toxicidad.5
La activación de los mecanismos innatos de defensa del sistema inmune, a través de inmunoestimulantes de origen natural y de eficacia comprobada, se presenta como una opción terapéutica innovadora en la prevención y tratamiento de la IRA.
Engystol®
Como una opción terapéutica de origen natural, se ha estudiado Engystol®, un medicamento inmunoestimulante que reduce significativamente la duración e intensidad de los síntomas durante la infección viral aguda (cuando se administra como tratamiento) y ayuda a proteger contra infecciones posteriores, hechos demostrados cientificamente.*
El Engystol® contiene dos principios activos fundamentales:
- Vincetoxicum hirundinaria (vencetósigo): estimulación sobre los mecanismos de defensa del huésped.
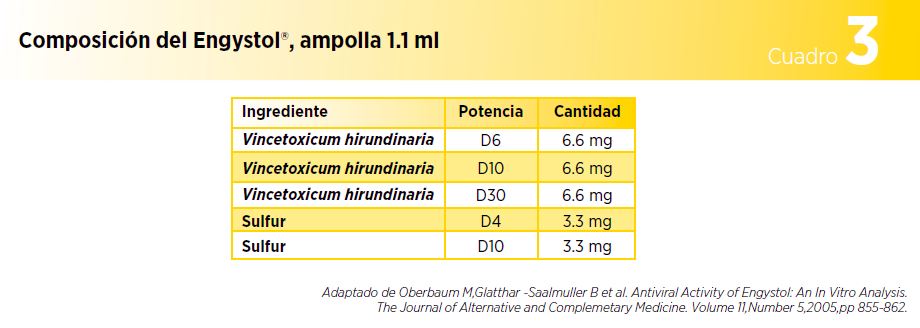
- Sulfur (azufre): a menudo, utilizado en las preparaciones homeopáticas para el manejo de diversas afecciones, como enfermedades cutáneas, inflamación aguda o crónica y trastornos hepáticos y gastrointestinales (ver Cuadro 3).5
Las presentaciones son en tabletas de uso sublingual y en ampollas inyectables (i.m., subcutánea e i.v.) (ver Cuadro 4).5
Aunque el mecanismo de acción aún no está completamente dilucidado, pruebas in vitro han demostrado que Engystol® interactúa con la cápside del virus, afectan la estructura de las proteínas de la cápside para enmascarar o alterar el epítope específico del virus y parece que influye sobre los componentes específicos de los virus necesarios para la replicación viral. Es muy posible que estén involucrados diferentes mecanismos con efectos antivirales.5
Pruebas in vitro han demostrado que Engystol® estimula la actividad fagocitaria de los granulocitos humanos en un 33.5%.1
Otros estudios demuestran que en el VSR se aumenta la capacidad fagocítica de los macrófagos.6 Su efecto sobre la inmunidad innata esta demostarda mediante el estudio de Roeska donde se observa un incremento importante del IFN alpha (Interferon Tipo 1) involucrado claramente en la actividad antiviral.7
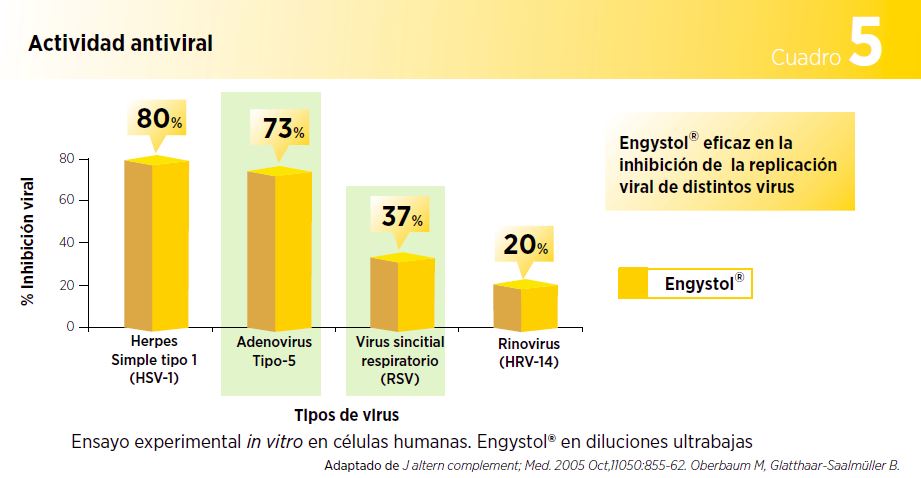
La investigación básica ha puesto de manifiesto la actividad de Engystol® frente a ciertos virus, como adenovirus de tipo 5, virus del herpes simple de tipo 1 (VHS 1) y virus respiratorio sincitial (VRS), así como frente al rinovirus humano (RVH).3 En el ámbito clínico, también se ha demostrado que Engystol® acorta el tiempo de infección y reduce los títulos de anticuerpos frente al virus influenza A. Estos resultados se observaron en un ensayo doble ciego, controlado con placebo, sobre prevención de la gripe (influenza) y el resfriado común (ver Cuadro 5).2
En el ámbito clínico, diversos estudios han demostrado su buena tolerabilidad, así como sus efectos antivirales terapéuticos y preventivos en casos de infección y de otras afecciones pulmonares con y sin fiebre, como bronquitis/asma, infecciones por VRS, infecciones de vías respiratorias altas, gripe, etc.2,8-12
El Engystol® tiene tanto usos preventivos como terapéuticos:
• Pacientes que sufren o son susceptibles de padecer una infección viral, como resfriado o gripe.
• Pacientes con enfermedades preexistentes, o mayores de 65 años que podrían ser más susceptibles a infecciones virales, por ejemplo, en invierno.
• Principalmente, niños pequeños sanos que podrían ser susceptibles a infecciones virales, por ejemplo, por VRS, en invierno.
• Toda la familia con infecciones virales.
Beneficios de Engystol®:
• Eficacia y seguridad científicamente demostradas y clínicamente probadas.
• Se puede utilizar tanto para tratamiento como para prevención de diversas infecciones virales.
• Estimula el sistema inmune específico e inespecífico (inmunoestimulante), y por lo tanto, lo fortalece.
• Seguro en mujeres embarazadas o madres lactantes, así como para toda la familia.
• No se ha descrito efectos secundarios, contraindicaciones o interacciones.
• Muy bien tolerado.
• Apto para tratamiento a largo plazo.
• Se puede asociar con otros tratamientos inmunoestimulantes naturales o convencionales.
Bibliografía:
1. Oberbaum M,Glatthar -Saalmuller B et al. Antiviral Activity of Engystol: An In Vitro Analysis. The Journal of Alternative and Complemetary Medicine.Volume 11,Number 5,2005,pp 855-862.
2. Enbergs H. Effects of the homeopathic Preparation Engystol on Interferon _ & Production by HUMAN T Lymphocytes. Immunological Investigations,35:19 27. 2006.
3. Bayona Y, Niederbacher J. Infecciones respiratorias virales en pediatría:generalidades sobre fisiopatogenia, diagnóstico y algunos desenlaces
clínicos. MÉD. UIS. 2015;28(1):133-141.
4. Protocolo de Vigilancia en Salud Pública de la Infección Respiratoria Aguda (IRA) 2016. Disponible en: http://www.ins.gov.co/lineas-deaccion/
Subdirecclon-Vlgilancla/sivlgilalProlocolos%20SIVIGILAlPRO%20Infeccion%20Respi ratoria%20Aguda% 201 RA.pdf.
5. Boletín Epidemiológico Semanal. Semana epidemiológica 13. Marzo 25 al 31 del 2018. Instituto Nacional de Salud Dirección de Vigilancia y Análisis del Riesgo en Salud Pública Publicación en línea: ISSN 2357-6189 2018.
6. Wronski S, Dannenmaier J, Schild S, Macke O, MuÈller L, Burmeister Y, et al. (2018) Engystol reduces onset of experimental respiratory syncytial
virus-induced respiratory inflammation in mice by modulating macrophage phagocytic capacity. PLoS ONE 13(4): e0195822.
7. Kerstin Roeska, Bernd Seilheimer. Antiviral activity of Engystol® and Gripp-Heel®: an in-vitro assessment. Roeska and Seilheimer. Journal of Immune Based Therapies and Vaccines 2010, 8: 6.
8. Wagner H et al. Influence of homeopathic drug preparations on the phagocytosis capability of granulocytes. Biol Ther 1993; XI(2):43-49.
9. Heilmann A. A combination injection preparation as a prophylactic for flu and common colds. Biol Ther 1994; VII(4):249-253.
10. Torbicka E, Brzozowska-Binda A, Wilczynski J, Uzerowicz A. RSV Infections in Infants: Therapy with a Homeopathic Preparation. Biomed Ther 1998;XVI(4):256260.
11. Matusiewicz R. The effect of a homeopathic preparation on the clinical condition of patients with corticosteroid-dependent bronchial asthma.
Biomed Ther 1997;XV(3): 70-74.
12. Herzberger G, Weiser M. Homeopathic Treatment of Infections of Various Origins: A Prospective Study. Biomed Ther 1997; XV(4):123-127.
13. Schmiedel V, Klein P. A et al. A complex homeopathic preparation for the symptomatic treatment of upper respiratory infections associated with the
common cold: an observational study. Explore 2006;2:109-114.
14. Denys A, Siewierrska K. Efficacy of preoperative immunoprophylaxis in patients with neoplastic diseases (II). Int Rev Allergol Clin Immunol
1999;5(1);46-50.

Material exclusivo para el profesional de la salud. © 2019 Circlepress. All rights reserved.